.gif)

-

-
2025 核心1型O(C1)多糖;2AB标记的标准品,Ludger货号: CAB-C1-01 参考价RMB 6700元(具体询价)
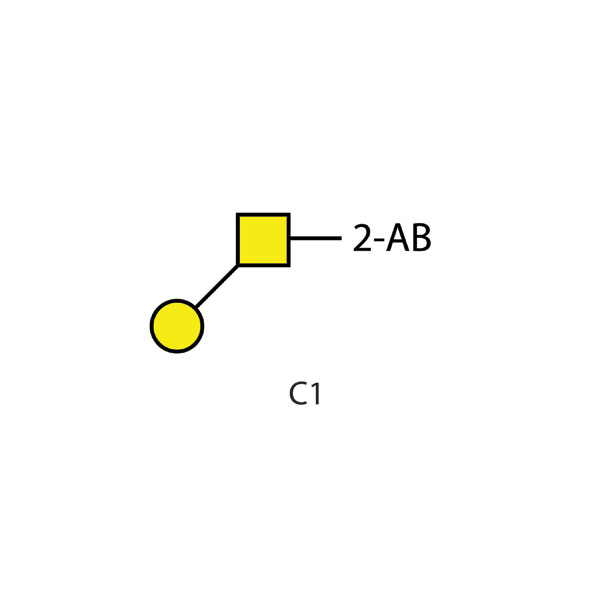
核心1型O(C1) 2-AB标记的多糖
半乳糖-β-(1-3)-N-乙酰半乳糖胺含末端半乳糖残基的线性核心1型O-聚糖,100皮摩尔
m/z: 503.2115产品说明书:
https://www.ludger.com/docs/products/cab/ludger-o-glycan-standards-overview.pdf
-
0.000.00
-
核心1型O(C1) 2-AB标记的多糖
半乳糖-β-(1-3)-N-乙酰半乳糖胺
含末端半乳糖残基的线性核心1型O-聚糖,100皮摩尔
m/z: 503.2115
产品说明书:
https://www.ludger.com/docs/products/cab/ludger-o-glycan-standards-overview.pdf
核心1型O(C1)多糖;2AB标记的标准品,Ludger货号: CAB-C1-01
核心1型O(C1)多糖;2AB标记的标准品,Ludger货号: CAB-C1-01
产品规格说明
核心1型与唾液酸化O-多糖标准品概述
核心1型O-多糖结构特征:
由β-1,3-半乳糖(Gal)分子连接至N-乙酰半乳糖胺(GalNAc)构成,经荧光标记分子2-AB(2-氨基苯甲酸)标记,适用于高灵敏度检测。
O-糖基化生物学背景:
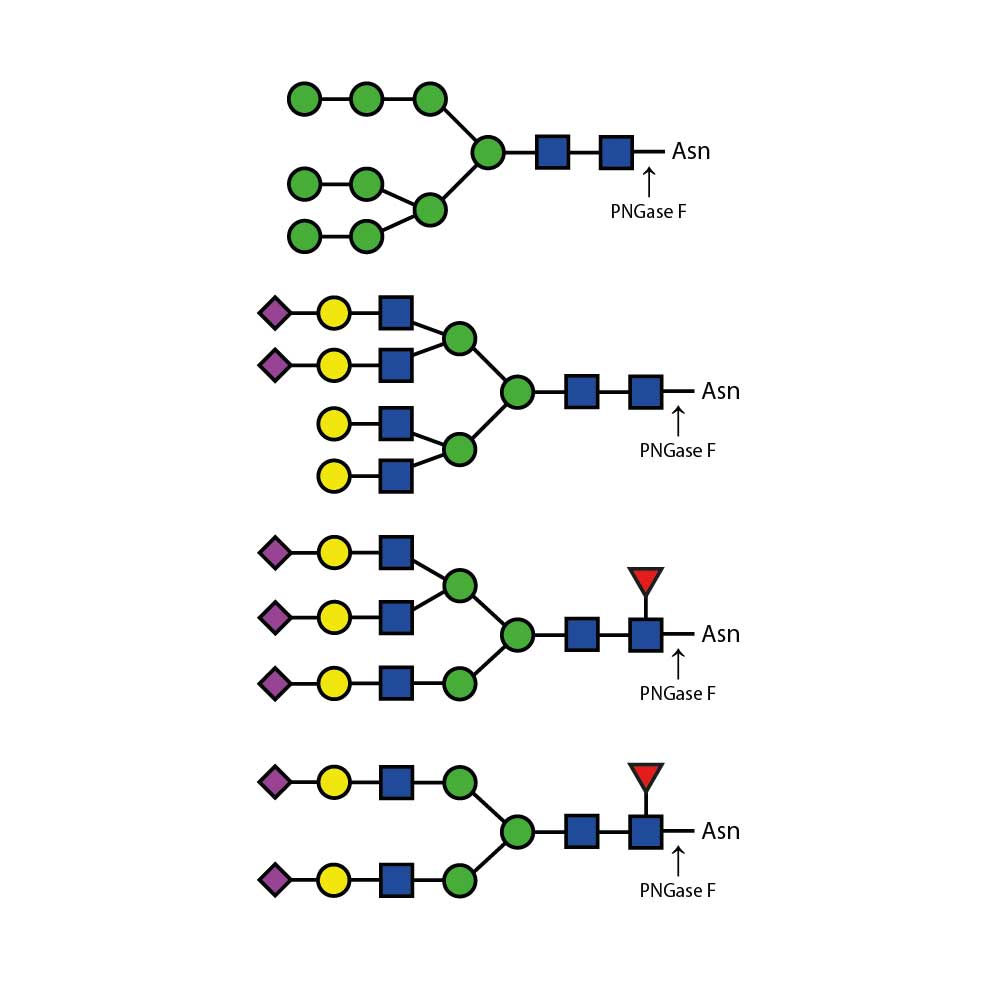
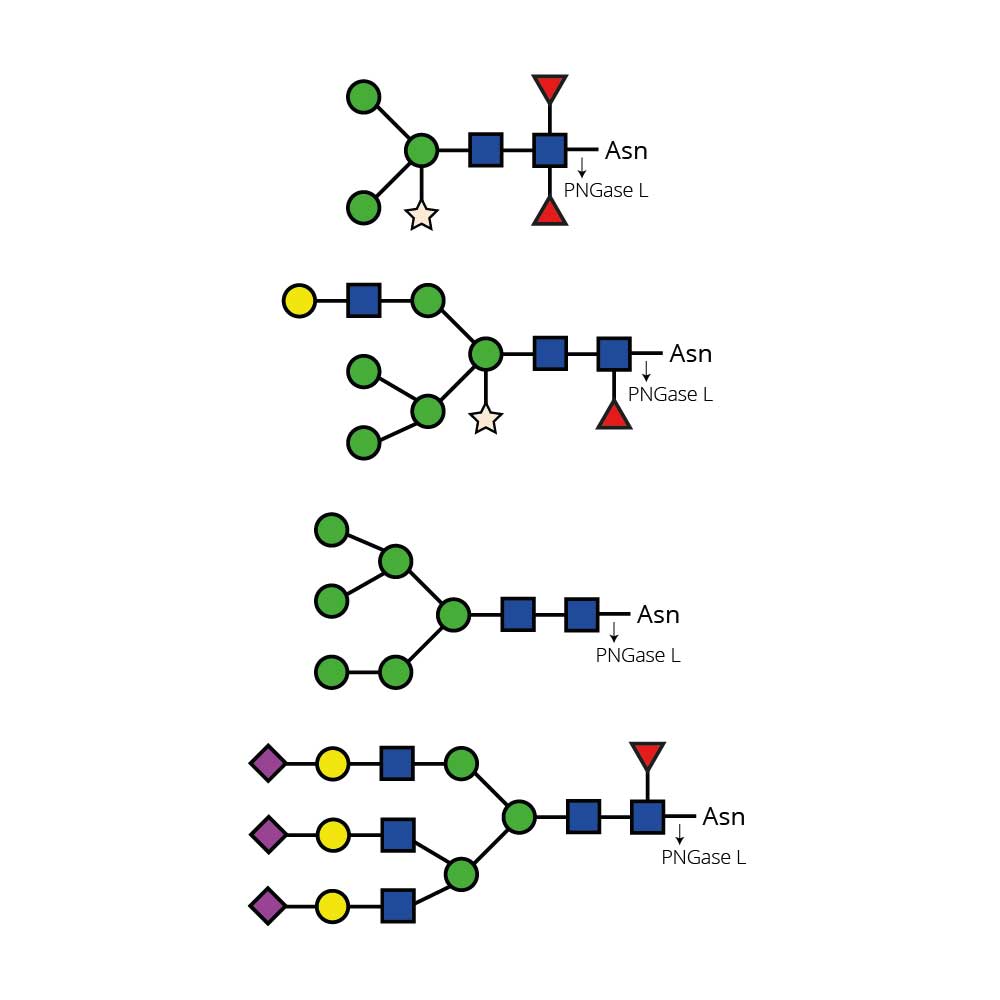
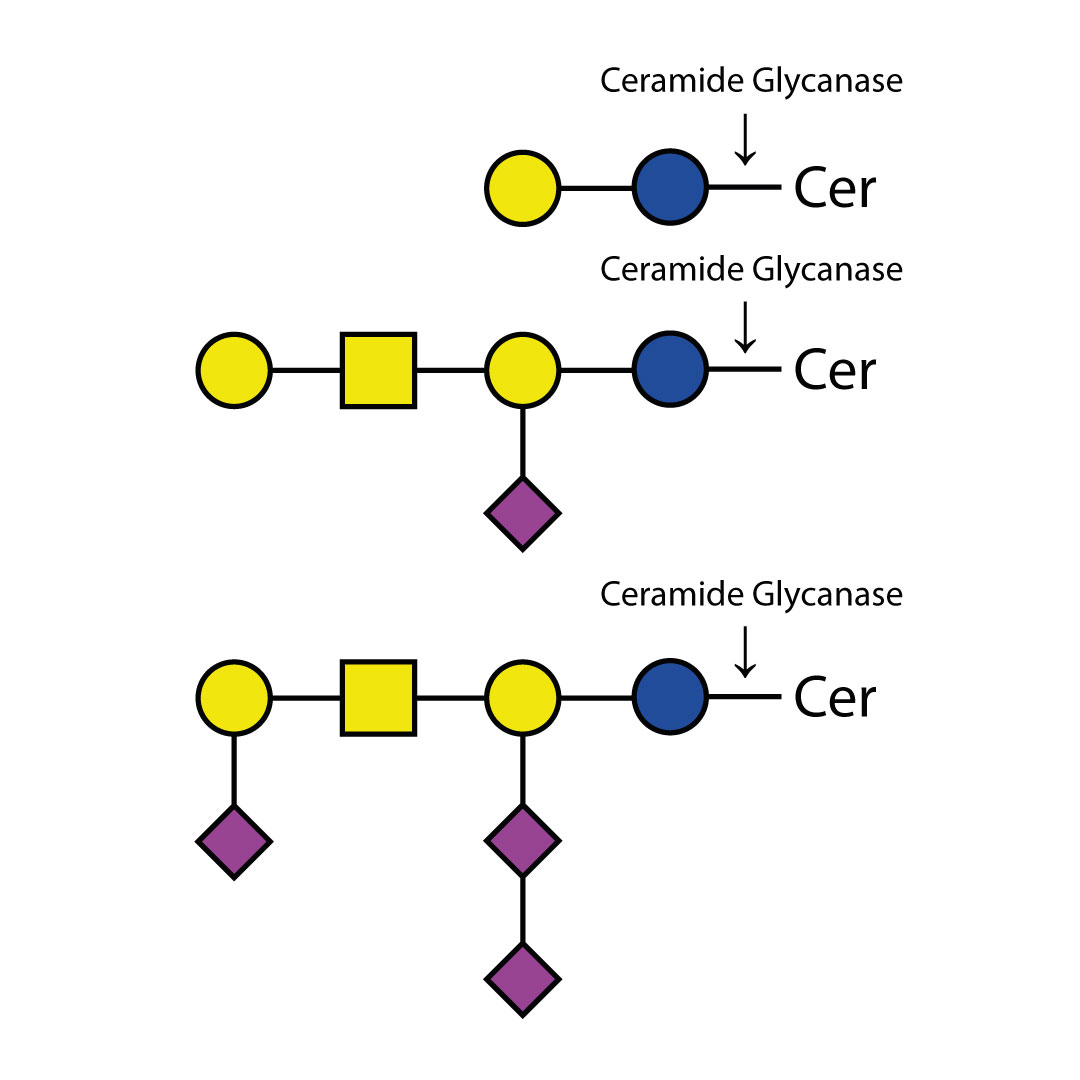
O-糖基化是哺乳动物糖蛋白(如分泌型糖蛋白及黏蛋白)中丝氨酸/苏氨酸残基的常见共价修饰形式。其核心结构形成路径如下:
1. 核心1结构:在GalNAc-Ser/Thr基础上,β-1,3-添加半乳糖(Gal)形成Gal-β1-3-GalNAc-α/β-O-Ser/Thr。
2. 核心2结构:在核心1结构基础上,β-1,6-添加N-乙酰葡萄糖胺(GlcNAc)进一步延伸。
目前已鉴定出**8种核心结构**,均可通过添加单糖(包括唾液酸)进一步延伸修饰。
生物药中的应用:
核心1型与核心2型O-糖链广泛存在于以下生物药中:
- 红细胞生成素(EPO)
- 依那西普(Enbrel,TNF-α抑制剂)
- 人凝血因子VIII(FVIII)
- 凝血因子IX
- 甘精胰岛素
2AB标记核心1型O(C1)多糖标准品详细参数
产品描述
2AB标记核心1型O-多糖(Core 1 O-Glycan, C1),纯度>90%(经CE-毛细管电泳与HPLC联合验证),适用于HPLC/UPLC分析中的峰归属及系统适用性测试。
规格参数
定量规格:100皮摩尔(100 pmol)
物理形态:冻干粉末,通过离心蒸发法从水溶液体系中干燥制得
纯度:>90%(CE-HPLC联合评估)
储存条件
- 溶解前/后均需保存于-20℃环境
- 未开封状态下稳定性≥5年
运输要求
- 冻干状态可常温运输
- 溶解后需干冰冷链运输
操作指南
1. 复溶前处理:
- 将未开封样品瓶恢复至室温,轻叩瓶底使冻干物聚集至瓶底
2. 复溶步骤:
- 缓慢开盖,加入适量复溶缓冲液(如50 mM ammonium bicarbonate, pH 8.0),重新密封后温和混匀
- 为确保最大回收率:
用复溶介质冲洗瓶盖内衬
复溶后短暂离心(3000 rpm, 2 min)去除颗粒
3. 关键注意事项:
- 所有玻璃/塑料器皿及溶剂需确保无糖苷酶残留及环境碳水化合物污染
- 避免暴露于高温(>30℃)或极端pH(<pH 6或>pH 9)环境
安全性
本产品为非危险品,原料经合成路径制备并认证,不含病原生物制剂等危害物质。
质量控制与合规性
- 纯度检测:采用HILIC-HPLC(亲水相互作用色谱)联合CE(毛细管电泳)双重验证
- 文件支持:每批次提供COA(质量分析证书)、HPLC/CE检测报告及SDS(安全数据表)
- 法规符合性:符合ISO 13485及GMP-like生产规范,适用于制药行业申报材料
3. 应用场景
(1) O-糖基化分析标准品
- 用于**核心1型O-糖链的定性/定量分析**,作为参照标准品校准仪器检测限与定量曲线。
- 支持**糖链异质性研究**(如不同唾液酸化/岩藻糖基化修饰的核心1型变体)。
(2) 生物药质量控制
- 单克隆抗体(mAb)与融合蛋白:部分治疗性蛋白(如抗VEGF抗体、EGFR靶向药)含O-糖基化位点,核心1型结构可影响其免疫原性、药代动力学(PK)及生物活性。
- ADC药物:抗体部分的O-糖基化可能干扰偶联效率或药物稳定性,C1标准品可用于工艺监控。
(3) 疾病标志物开发
- 核心1型O-糖链的异常修饰(如Tn抗原/GalNAcα1-O-Ser/Thr)与**癌症(如结直肠癌、乳腺癌)、自身免疫疾病**相关,C1可作为**早期诊断标志物开发**的参照。
核心1型O-多糖在单抗药物中的关键作用以及对ADC药物性能的影响
单抗药物核心1型O-多糖分析
1. 核心1型O-多糖在单抗药物中的关键作用
核心1型O-多糖(Gal-β1-3-GalNAc-α/β-O-Ser/Thr)是单克隆抗体(mAb)中黏蛋白型O-糖基化的主要结构之一,主要分布于抗体的Fc段(恒定区)和部分Fab段(可变区)。其糖基化修饰(如唾液酸化、岩藻糖基化、半乳糖基化等)直接影响单抗药物的以下功能:
ADCC(抗体依赖性细胞介导的细胞毒性)效应:
- **核心1型基础结构**(未进一步修饰)可能降低ADCC活性;
- 若核心1型进一步延伸并携带**唾液酸**(如sialylated-Core1),可显著增强ADCC效应,提升对肿瘤细胞的杀伤能力。
- CDC(补体依赖性细胞毒性)效应:
- 核心1型糖链的半乳糖基化程度影响补体成分(如C1q)的结合能力,进而调控CDC活性。
- 药代动力学(PK):
- 唾液酸化修饰可延长单抗在血液中的半衰期(减少肾小球滤过清除);
- 岩藻糖基化会降低与FcγRIIIa受体的结合亲和力,间接影响PK。
- 免疫原性风险:
- 异常的核心1型糖链(如Tn抗原暴露,GalNAc-α-O-Ser/Thr)可能引发机体免疫反应,导致抗药物抗体(ADA)产生。
3. 工艺控制与质量标准
关键质量属性(CQAs):
- 核心1型O-糖链的含量(通常要求占总O-糖链的10%-30%);
- 唾液酸化比例(影响ADCC/CDC效应);
- 岩藻糖基化水平(关联FcγRIIIa结合亲和力)。
- 工艺优化方向:
- 通过调整细胞培养条件(如温度、pH、添加唾液酸前体)调控核心1型糖链的修饰;
- 使用糖基化工程化细胞株(如敲除岩藻糖基转移酶基因)降低岩藻糖基化水平。
ADC药物核心1型O-糖链的应用
(抗体偶联药物中的糖基化影响)
1. 核心1型O-多糖对ADC药物性能的影响
ADC药物(抗体偶联药物)由单抗通过连接子(Linker)与小分子药物(如微管抑制剂、DNA损伤剂)偶联而成。核心1型O-糖链虽位于抗体部分,但其修饰状态可间接影响ADC药物的以下特性:
- 偶联效率:
- 核心1型糖链的**空间位阻效应**可能干扰连接子与抗体Fc段的偶联位点(如赖氨酸或半胱氨酸残基),导致偶联率降低;
- 唾液酸化修饰可能增加抗体表面的负电荷,影响连接子的静电吸附效率。
- 药物稳定性:
- 核心1型糖链的**唾液酸化**可延缓ADC药物在血液中的清除(延长半衰期),但过量唾液酸可能导致非特异性结合(如与肝脏唾液酸受体结合),增加脱靶毒性;
- 岩藻糖基化降低FcγR结合能力,可能减少ADC药物在免疫细胞内的内化,影响药物释放效率。
- 疗效与安全性:
- 核心1型糖链的异质性(如不同唾液酸化程度)可能导致ADC药物在肿瘤组织中的分布不均,影响疗效;
- 异常核心1型糖链(如Tn抗原暴露)可能增加免疫原性风险,引发ADA产生,降低药物持久性。
案例:核心1型O-多糖与ADC药物优化
某HER2靶向ADC药物在临床前研究中观察到:
- 高唾液酸化的核心1型O-多糖导致药物在肝脏中的非特异性蓄积(ALT/AST升高);
- 通过调整细胞培养基中的**唾液酸前体浓度**,降低核心1型糖链的唾液酸化比例后,药物肝脏毒性显著减少,同时肿瘤靶向性提高(ORR从40%提升至65%)。
Ludger 是一家位于英国专门从事药物的糖基化分析和研究的生物科技公司。
我们可以为制药公司进行设计、测量以及控制药物糖基化的安全性和有效性。
公司技术是用在FDA的质量控制和EMEA批准的全球生物制药,可用于支持IND申报。
Ludger的客户包括世界各地top的制药公司和生物技术公司。
Ludger药品生产涵盖了全面符合ICH-生物制药的糖基化分析试剂和检测试剂盒。
产品包括多糖释放试剂盒、多糖标记和纯化试剂盒、标记聚糖、多糖HPLC柱、内糖苷酶和糖蛋白标准品等。同时Ludger会继续开发新的产品,以确保为您提供更高品质产品。
此外,我们还为客户提供糖基化分析、培训以及相关的产品和服务等。
您可以通过不同的方式使用我们糖基化分析服务。我们可以帮助您选择适合您需求的最佳方法。我们有多年的专业经验进行糖蛋白中N-和O-聚糖分析,糖蛋白包括:单克隆抗体、Fc融合蛋白、促红细胞生成素以及其他治疗性糖蛋白。
英国Ludger生物科技有限公司中国办事处
电 话: (Cindy):157 1167 5909 & (Lily)186 0210 8329
QQ(Lily): 258363 672 QQ(Cindy): 170 439 096
邮 箱:lily.wang@ludger.com & cindy.li@ludger.com
网站:Ludger中文官网 www.ludgersh.com www.ludger.com
电话:186 0210 8329
157 1167 5909
cindy.li@ludger.com
QQ:258363672 170439096
Ludger

QQ(Lily): 258363 672 QQ(Cindy): 170 439 096
地 址:上海静安区南京西路1266号